导语
研究载体颗粒在细胞膜表面的动态搜寻行为以及载体颗粒与细胞膜表面受体动态相互作用规律,将有助于揭示载体颗粒的跨膜运输机制,从而为设计低毒高效的靶向纳米药物提供理论依据。近日,中南大学化学化工学院肖乐辉教授在该领域取得进展,相关研究成果发表在J. Am. Chem. Soc.(DOI: 10.1021/jacs.3c06925)
前沿科研成果
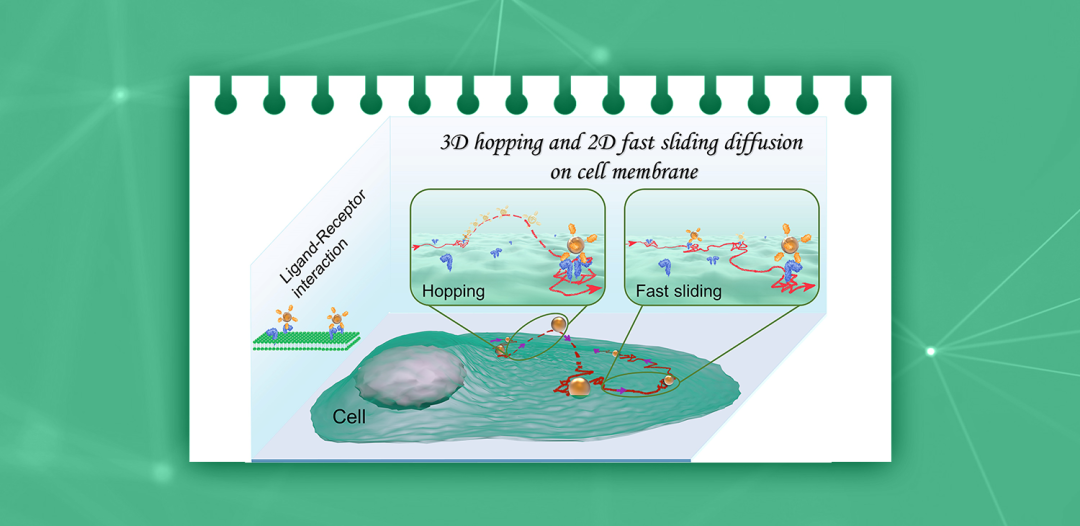
配-受体相互作用触发细胞膜表面跳跃和滑行扩散
纳米载体在活细胞膜表面的扩散动力学与配-受体相互作用密切相关,决定了细胞内化效率。然而,细胞膜表面冗杂的生物大分子会干扰受体的搜寻和识别过程,并影响载体颗粒在活细胞膜上的扩散途径。纳米载体在细胞膜表面的运动迁移通常以三维(3D)方式进行,包括3D跳跃和2D快速滑行特征,涉及与多个受体之间的远程弱相互作用。这些迁移模式由粘性阻力、分子热运动以及配体和受体之间的分子结合共同作用。探索纳米载体颗粒在活细胞膜上的迁移行为对理解跨膜过程至关重要。为此,多种成像方法被应用于扩散过程分析,包括暗场显微镜(DFM)、微分干涉相差显微镜、共焦显微镜和干涉散射显微镜。
在这些技术中,DFM由于光学元件简单而成为最受推崇的方法。然而,该技术的一个关键掣肘是DFM通常利用透射照明模式进行样品激发。在视窗范围内,与附近周围环境具有明显折射率差异的物体均会产生散射信号。在这种情况下,如何在高信噪比条件下选择性地分辨目标标本是一个巨大的挑战,特别是在活细胞环境中。此外,目前的研究多集中在2D扩散动力学研究,对瞬态扩散中3D跳跃和2D快速滑行行为的解析仍然匮乏。
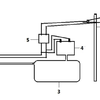
基于此,该团队发展了一种全新的白光源全内反射散射成像技术,在无需引入额外光学元件下,通过逐渐减小激发光路中的光阑尺寸,可准确调控入射光束的角度,在普通暗视野光学显微镜上便可实现全内反射散射(TIRS)照明。
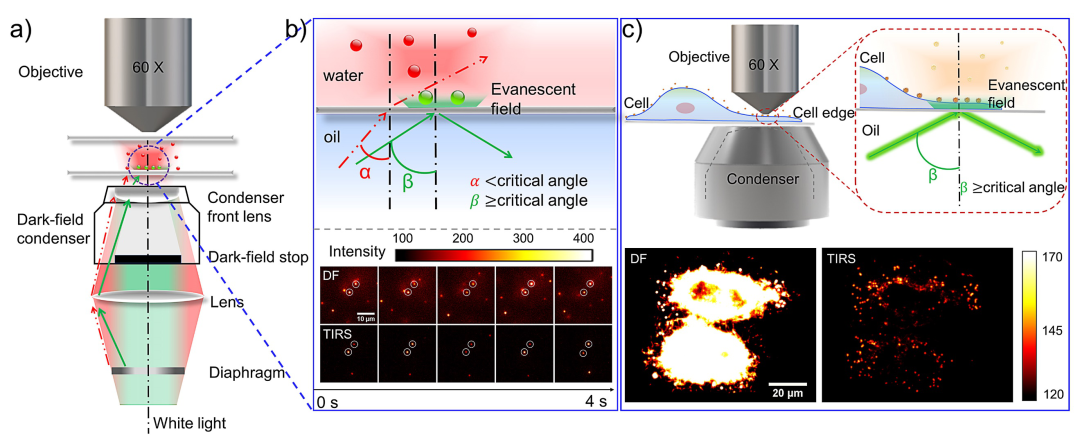
图1 基于传统暗场显微镜的TIRS成像原理图(图片来源:J. Am. Chem. Soc.)
利用该成像方法,选择性地监测了活细胞膜上转铁蛋白修饰的纳米颗粒的运动迁移行为。通过对载体颗粒(TGNPs-1和TGNPs-2)在细胞膜表面运动过程扩散动力学分析发现,在细胞膜表面结合位点的动态识别过程中,载体颗粒的迁移呈现受限扩散和长程搜索之间的动态切换,表现出非高斯和各态非遍历性特征。
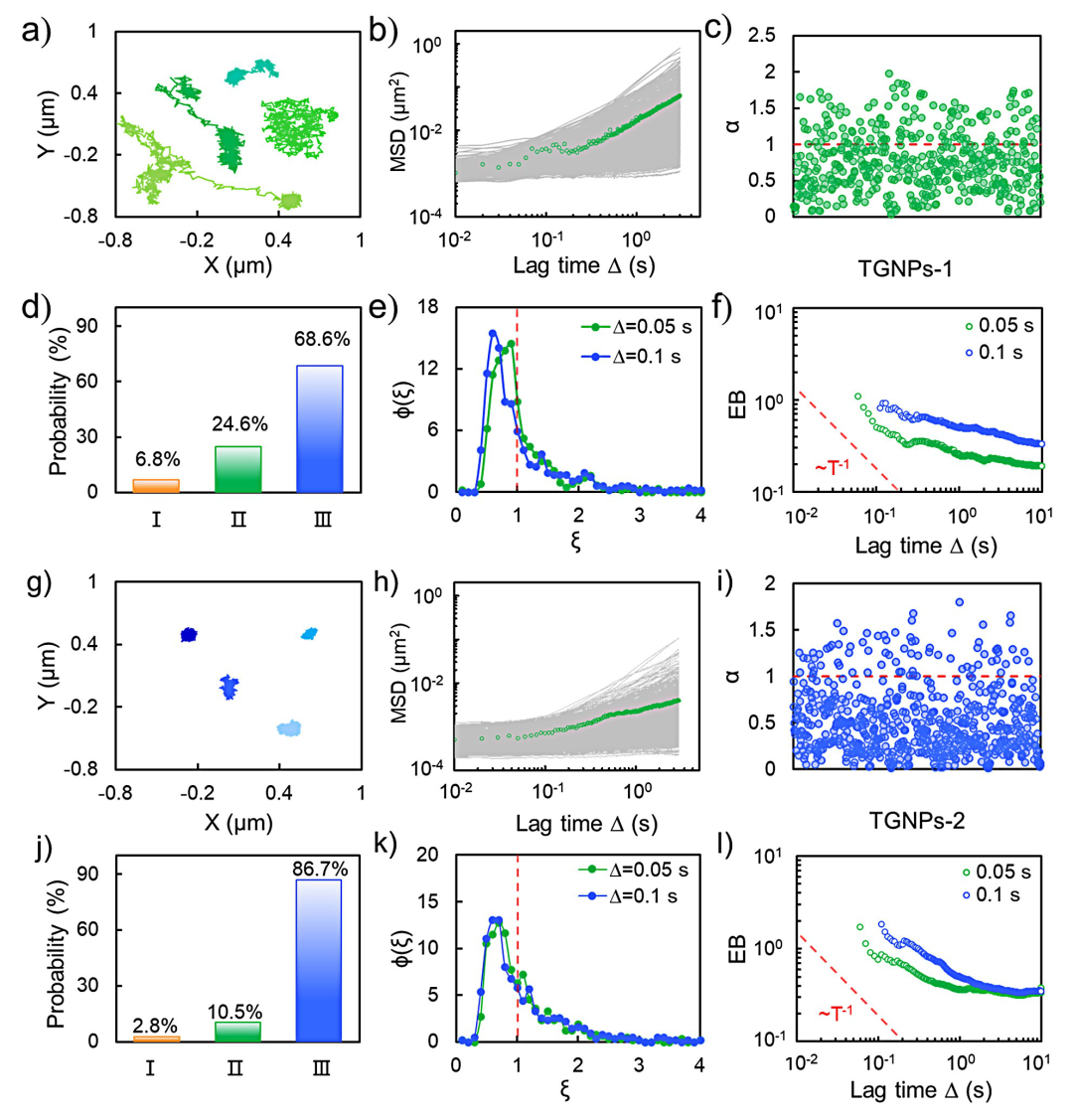
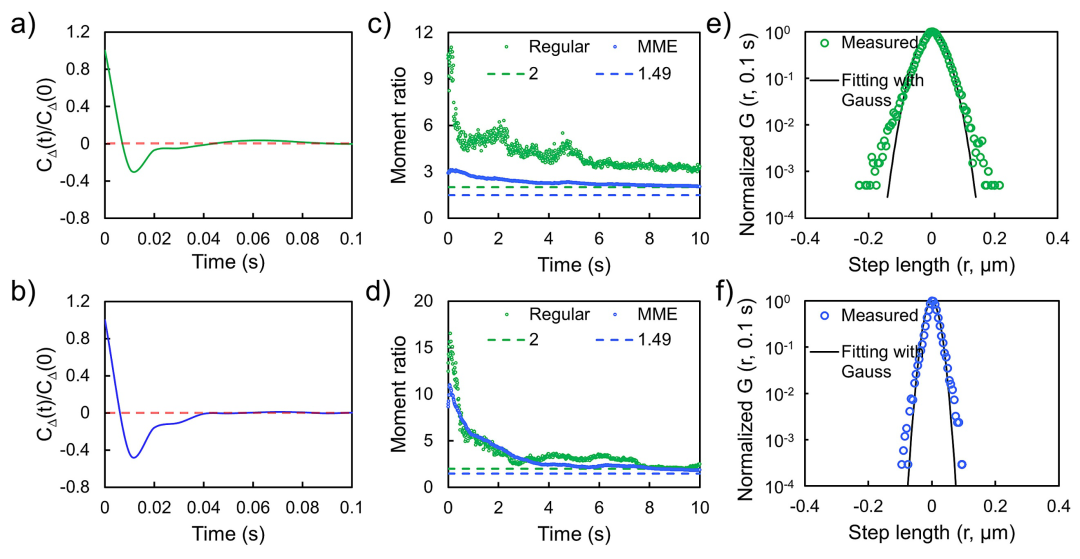
图3. 纳米载体在活细胞膜上的扩散机制分析(图片来源:J. Am. Chem. Soc.)
此外,通过测量纳米载体在活细胞膜表面沿着Z轴方向的位移和自由能图谱分析,首次揭示了载体颗粒在细胞膜表面的2D快速滑动和3D跳跃扩散行为。这一系列复杂运动行为间的切换主要受配体与受体相互作用强度的调节。
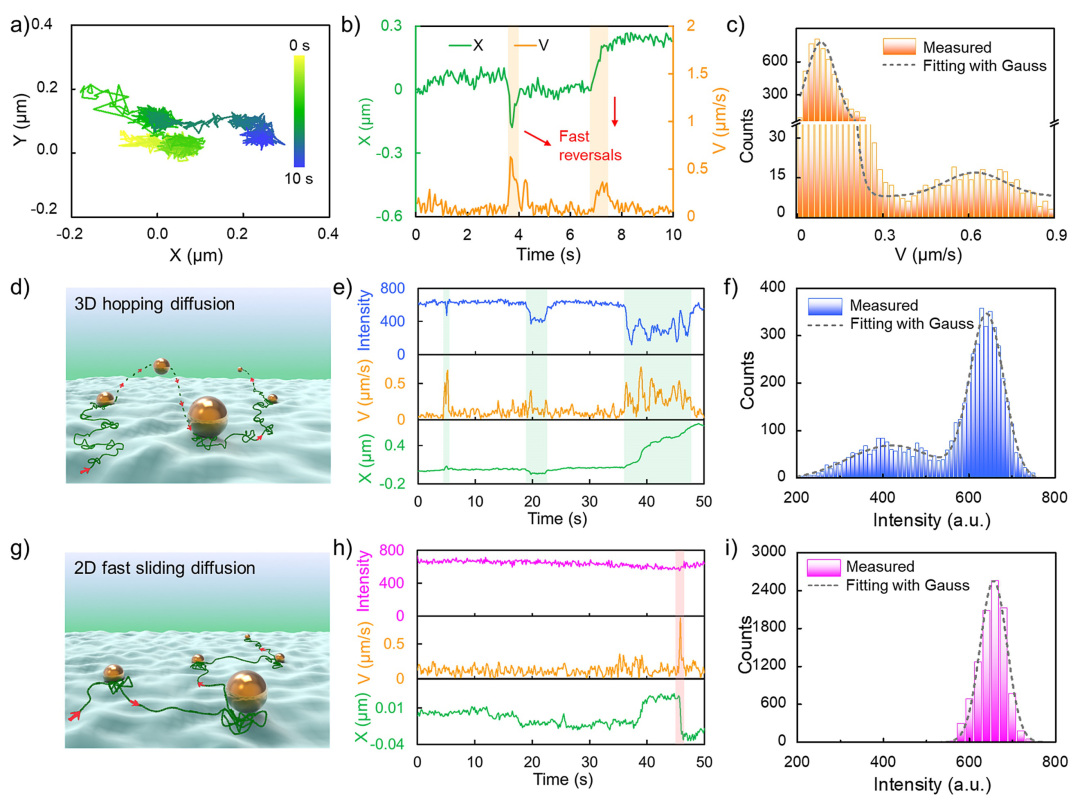
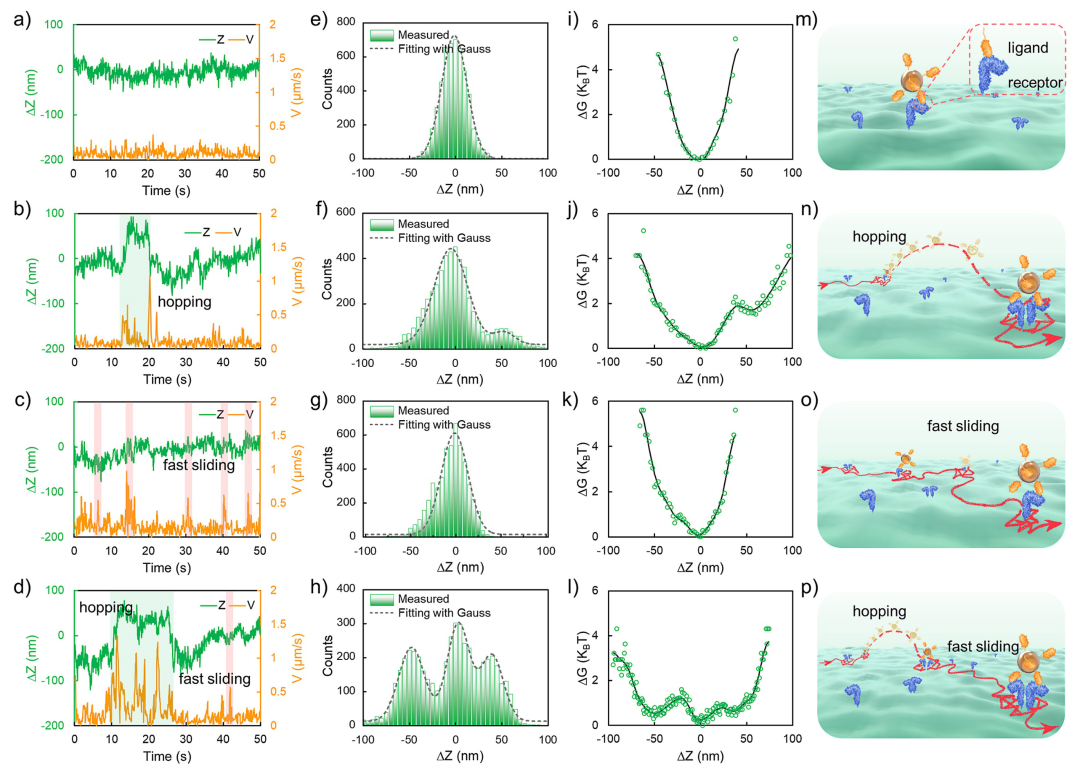
图5 纳米载体在活细胞膜表面瞬态结合过程的自由能分析(图片来源:J. Am. Chem. Soc.)
在该研究中,作者通过减小激发光路中的光阑尺寸,可准确调控入射光束的角度,在普通商业暗场光学显微镜上实现全内反射散射(TIRS)照明。通过该方法,选择性地监测了活细胞膜上转铁蛋白修饰的纳米颗粒的运动迁移行为。单颗粒动态追踪研究结果表明,TGNPs在细胞膜表面的动态迁移过程具有时空异质性,具有非高斯和各态非遍历性。通过Z轴位移和自由能图谱分析,可以准确区分载体颗粒在细胞膜表面的3D跳跃和2D快速滑动扩散模式。这些研究结果对膜表面受体介导的物质运输机制的理解具有一定的指导性意义。
本篇工作的通讯作者为中南大学化学化工学院肖乐辉教授,第一作者为郑州大学化学学院叶中菊研究员。上述研究工作得到了国家自然科学基金(No. 22174079,21974073,22204147)和河南省自然科学基金(No. 222300420288)的支持。